

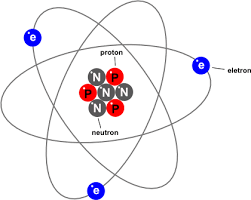
Quem descobriu o elétron foi Joseph Thomson e em estudos futuros Rutheford e Bohr, o elétron é uma partícula subatômica que tem carga negativa e se localiza na eletrosfera, em torno do núcleo atômico, o que decorre da força eletromagnética. Um átomo tem sua eletrosfera divida em camadas, a quantidade de camadas está na Tabela Periódica através do periodo que o elemento está. São no máximo 7 camadas (K, L, M, N, O, P, Q). A ultima camada do átomo é chamada de camada de valência.

| Categoria | Elemento | Símbolo | Número Atomîco | Distribuição |
|---|---|---|---|---|
| Gases Nobres | Hélio - He | 2 | 1s² | |
| Ametais | Carbono- C | 6 | 1s² 2s² 2p² | |
| Cloro -Cl | 17 | 1s² 2s² 2p6 3s² 3p5 | ||
| Oxigênio - O | 8 | 1s² 2s² 2p4 | ||
| Nitrogênio - N | 7 | 1s² 2s² 2p³ | ||
| Metais Alcalinos | Magnésio - Mg | 12 | 1s² 2s² 2p6 3s² | |
| Berílio - Be | 4 | 1s² 2s² | ||
Através do diagrama de Linus Pauling, é possível fazer a Distrubuição de quantos elétons ficam em cada camada.
Veja ao lado o diagrama, e abaixo veja a Distrubuição Eletrônica de alguns elementos da Tabela Periódica: